#Kuantum Kimya: Moleküller Nasıl Oluşuyor?

Inhaltsverzeichnis
„Kuantum Kimya: Moleküller Nasıl Oluşuyor?“
 Atomlar neden moleküller oluÅturuyor ve insanlara yaÅam veren organik moleküller nasıl oluÅuyor? Tamam, evrendeki bütün fiziksel sistemler en düÅük enerji durumuna geçmek ister ama birçok atomdan oluÅan bir molekülün enerjisinin tek tek atomlardan fazla olması gerekmiyor mu? Ãyleyse atomlar neden birleÅip bize hayat veren su ve hemoglobin gibi moleküller oluÅturuyor? Kuantum kimya ile kimyasal baÄların kuantum fiziÄini görelim.
Atomlar neden moleküller oluÅturuyor ve insanlara yaÅam veren organik moleküller nasıl oluÅuyor? Tamam, evrendeki bütün fiziksel sistemler en düÅük enerji durumuna geçmek ister ama birçok atomdan oluÅan bir molekülün enerjisinin tek tek atomlardan fazla olması gerekmiyor mu? Ãyleyse atomlar neden birleÅip bize hayat veren su ve hemoglobin gibi moleküller oluÅturuyor? Kuantum kimya ile kimyasal baÄların kuantum fiziÄini görelim.
YaÅam için kuantum kimya
Bu yazı yaÅamın kuantum kökenini açıklayan kuantum biyoloji ve suyun yaÅam için neden kritik olduÄunu anlatan su kimyasının devamıdır. Mademki atomların kuantum mekaniÄini gördük, öyleyse bugün de moleküllerin kuantum kimyasını görelim. ? Ãyle ya, nükleer reaktörlerde üretilenleri saymazsak doÄada yaklaÅık 100 element yani 100 farklı atom bulunuyor. Oysa bunların oluÅturduÄu moleküllerden astrofizikteki yıldızlar ve kara delikler gibi çok çeÅitli ürünler çıktıÄını görüyoruz.
Evet, kuantum kimya galaksilerden baÅlayarak bütün gökcisimlerinin oluÅumunda önemli bir rol oynuyor. Oysa canlıların yani biyokimyanın yanında astrofizik çok basit kalıyor ki tekrar ediyorum; siz, ben, yıldızlar ve seçildikten sonra her yeri Adana yapan Trump az veya çok, farklı atomdan oluÅuyoruz. Trilyonlarca deÄiÅik molekül üreten ~100 atom! Peki biz maddenin bu en basit yapıtaÅlarından nasıl türedik? Bu soru pratikte yaÅam cansız Dünyaâda 4 milyar yıl önce nasıl ortaya çıktı sorusuna denktir.
Biyokimya kuantum kimyadan ve o da atomlar arasındaki kimyasal baÄlardan baÅlar. Moleküller kimyasal baÄlarla birbirine baÄlanan atomlardan meydana geldiÄi için moleküllerin oluÅumunu da kimyasal baÄlarla anlatacaÄız. Nedir bunlar ve kuantum mekaniÄinde nasıl çalıÅır?
İlgili yazı: Kodlama İçin En Gerekli 16 Programlama Dili
RESİM 1. Büyütmek için tıklayın.
Atomlar ve moleküller
Ãncelikle atomlar nadiren tek baÅına bulunur. En basit element olan hidrojen atomları bile uzayda yan yana gelerek moleküler hidrojen oluÅturur. Keza atmosferde hava diye soluduÄumuz oksijen de moleküler oksijen formundadır. Atomların kimyasal baÄları basit ama ürettiÄi moleküller o kadar karmaÅık olabilir ki evrende gördüÄümüz her Åeyi bunlara borçlu oluruz.
Canlı türleri, insan bünyesi (metabolizma), enerji üretiminde kullandıÄımız yakıtlar, bilinçsiz beyinden çıkan bilinç ve bizi büyük ölçekte etkileyen diÄer her Åey moleküllerin eseridir ancak bunu daha net ifade edelim: Moleküler atomların fiziksel özellikleri tekil atomlardan farkıdır. Moleküler özelliklere kimyasal özellikler deriz ve bu farklılık sayesinde moleküller canlı dokular gibi atomların üretemediÄi malzemeler üretirler. Neden derseniz kuantum mekaniÄi sayesinde:
Ä°lgili yazı: Gerçek Adem: ilk insan ne zaman yaÅadı?
RESİM 2. Büyütmek için tıklayın.
Kuantum kimya ve hidrojen
SoluduÄumuz hava ve içtiÄimiz su tekil atomlar yerine moleküllerden oluÅur. Atmosferin aÅırı oksijenlenerek akciÄerlerimizi yakmasını önleyen azot atomları bile moleküler azot (N2) olarak bulunur. Moleküler oksijenle azot ikiÅer atomdan ve su molekülü de bir hidrojen atomuyla iki oksijen atomundan oluÅur ama atomların neden birbirine baÄlandıÄını merak ediyorsanız kök sebebi enerjidir:
Bütün doÄal sistemler en düÅük enerji düzeyine geçmek ister. ÃrneÄin bir tepenin doruÄundaki topun potansiyel enerjisi yüksek olup yamaçtan aÅaÄı yuvarlanmaya eÄilimlidir. YuvarlanacaÄı vadinin en çukur noktası ise daha düÅük potansiyel enerjiye sahip olacaktır. Irmaklar bu yüzden denize akar; çünkü deniz her zaman karalardan alçaktır.
Peki enerji moleküllerin oluÅumunda nasıl bir rol oynuyor? Bunu yalnızca bir proton (çekirdek) ve elektrondan oluÅan en yalınç element olan hidrojenle görelim. Hidrojen atomları uzayda moleküler hidrojen yani gaz olarak bulunur. Atomların kuantum mekaniÄinde gördüÄümüz gibi hidrojen çekirdeÄi çevresinde dönen tek elektron yine de bir elektron bulutu oluÅturur.
Heisenbergâin belirsizlik ilkesi gereÄi elektronun kesin yörüngesini bilemeyiz ama büyük olasılıkla nerelerde olabileceÄi bellidir. Bunlar olası yörünge çizgilerinin yani yörüngemsilerin yün yumaÄını andıran toplamıdır. Dahası yörünge bulutunun Åekli de Schrödinger dalga fonksiyonu ile belirlenir.
Moleküllerin doÄuÅu
Ãyle ki hidrojen atomunun Schrödinger dalga fonksiyonu elektron ve protonun birlikte alabileceÄi bütün birleÅimleri gösterir. Biz de ölçüm yaptıÄımız bunlardan birini görürüz. Tekil hidrojen atomları en düÅük enerji düzeyinde yani taban durumundadır ancak mevcut atoma baÅka bir atom yaklaÅtıÄı zaman moleküllerin oluÅumuyla ilgili çok ilginç Åeyler olur:
Ä°lgili yazı: Düz Dünya Teorisini Ãürüten 12 Kanıt
RESİM 3. Büyütmek için tıklayın.
Kuantum kimya ve atom baÄları
Ä°lk olarak elektromanyetik kuvvette zıt yükler birbirini ittiÄi için yaklaÅan atomları saran eksi yüklü elektronlar birbirini iter. Oysa birbirine yaklaÅan elektronlar karÅı atomun çekirdeÄini oluÅturan protonun pozitif yükünden de etkilenir ki elektromanyetik kuvvette zıt yükler birbirini çeker. Sonuç olarak elektronlar hem birbirini iter hem de karÅılıklı protonlar tarafından çekilir.
Atomlar birbirine çok yaklaÅırsa protonların itici etkileÅimi ve çok uzaklaÅırsa elektron ve protonların çekici etkileÅimi baskın çıkacaktır. Dolayısıyla atomların arasındaki uzaklık açısından bir denge kurulur. Bu denge proton ve elektronların eÅlerini itmesiyle karÅılıklı birbirini çekmesi arasındaki dengedir. Aynı zamanda iki atomun birbirine yakın olabileceÄi en düÅük enerji düzeyine karÅılık gelir.
Dolayısıyla iki atomun en düÅük enerji düzeyi itici ve çekici etkilerin bileÅimiyle belirlenir ki bu uygun uzaklıkta atomlar sahip olduÄu elektronları ikisi arasında paylaÅmaya baÅlar yani elektronlar iki atom çevresinde birden dönmeye baÅlar. Åimdi diyeceksiniz ki âAma hocam, hidrojen atomları neden daha baÅtan birbirine yaklaÅtı? Elektronların birbirini itmesi yüzünden hiç yaklaÅmamıŠolmaları gerekmez mi?â Ãok doÄru bir soru ve cevabı kuantum mekaniÄi ile kuantum tünellemede yatıyor:
Ä°lgili yazı: Virüsler Canlı mı ve RNA YaÅamın kökeni mi?

RESİM 4. Büyütmek için tıklayın.
Â
Kuantum tünelleme ve moleküller
Neden atomlar çok yaklaÅırsa protonların birbirini itmesi ve çok uzaklaÅırsa elektronlarla protonların birbirini çekmesi baskın çıkıyor? Bunun nedeni kuantum tünellemedir ki ne olduÄunu önceki yazıda anlattım ama özetle elektronlar birbirine uygun uzaklıkta olan atomlar arasında kuantum tünelleme ile gidip gelir ve atom yörüngelerini böyle paylaÅır.
Kuantum tünelleme elektronların kısa mesafelerde çekirdeklerine doÄru ıÅınlamalarına izin verir fakat bu belirsizlik ilkesi yüzünden rastgele gerçekleÅen bir süreçtir yani dengesizdir. Dengesiz derken elektron tünelleme modelinde bu parçacıklar sıvı gibi akar ve çekirdeklerin çevresinde yoÄuÅarak molekülün potansiyel enerjisini düÅürür. Aynı zamanda çekirdekler arasında akarak kinetik enerjiyi düÅürür. Bu da atomları baÄlayan kimyasal baÄın gelgitli olmasını, Åiddetinin deÄiÅmesini saÄlar.
Dolayısıyla atomlar yalnızca uygun uzaklıktaysa elektronlar baÄlayıcı olarak moleküller oluÅturur ama atomlar çok yakınsa protonların birbirini itiÅine yenik düÅer (Ãniversitede kuantum kimya okuduysanız biliyorsunuz ? ama liseye de girdi mi, bilmiyorum. Ben 94 mezunuyum, benim zamanımda yoktu).
Ãzetle atomların birbirine uygun uzaklıkta moleküller oluÅturmasını saÄlayan potansiyel enerji sistemin tamamının potansiyel enerjisidir ve aslında kinetik enerjiyle kurulan bir dengedir. Bu enerji dengesi üç faktörden etkilenir: 1) Atomların tekil kinetik enerjisi, 2) Ä°ki proton arasındaki potansiyel enerji (itici güç), 3) iki elektron arasındaki potansiyel enerji (itici güç) ve 4) Elektronlarla protonlar arasındaki potansiyel enerji (çekici güç). Sonuç olarak moleküller ekolayzır gibidir:
İlgili yazı: İnternetinizi Uçuracak En İyi 10 Modem
RESİM 5. Büyütmek için tıklayın.
Kuantum kimya ekolayzırı
Moleküller 4 bant ekolayzır (eÅitleyici) gibidir ve yukarıdaki dört faktörü dengelerseniz kararlı bir molekül oluÅturmuÅ olursunuz. Bu ekolayzırın ayarları Schrödinger dalga fonksiyonu uyarınca yapılır. Biz de bu kuantum sisteminin kinetik ve potansiyel enerjisini Hamiltonyan denklemi ile hesaplarız (Resim 4). Ä°ki hidrojen atomundan oluÅan moleküler hidrojenin Hamiltonyanı ise resimdeki gibidir ancak son bir etmen var:
Her elementin elektron ve proton sayısı farklıdır. Ä°zotopların da nötron ve proton sayısı farklıdır. Bu nedenle soy gazlar gibi kimyasal reaksiyona girmeyen ya da halojenler gibi tepkimeye dünden teÅne olan elementler belirir. Kısacası moleküllerin kararlı olup olmayacaÄı elektron sayısıyla belirlenir. Hamiltonyan, sistemin enerjisine karÅılık gelen bir operatördür ve bunu zamandan baÄımsız Schrödinger denklemine eklediÄiniz zaman resimdeki gibi olası enerji düzeylerini hesaplayabilirsiniz.
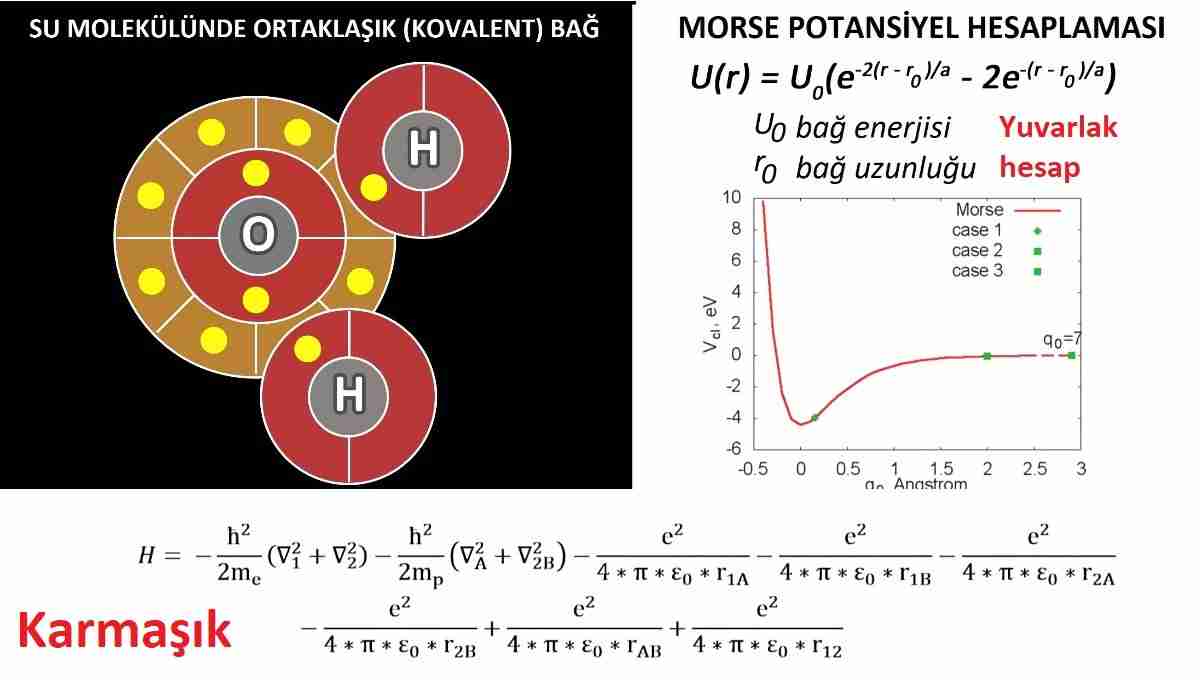
Nitekim kimyasal baÄların en düÅük enerji düzeyinden kasıt sistemin toplam enerji düzeyinin minimum genliÄidir. Hamiltonyan iÅte bunu hesaplamanızı saÄlar ama bunu anlamak için biraz da bilimsel terimlerin kökenine bakalım: Kimya sınavlarının belalısı kovalent baÄ ne demektir? Sözlüklerde bunun ortaklaÅık baÄ olarak çevrildiÄini görüyoruz ama baÅka bir karÅılık kullanabiliriz.
Kovalent eÅdeÄerli baÄ demektir yani molekül sisteminin enerji düzeyinin elektronlar sayesinde iki atom arasında neredeyse eÅit olarak paylaÅılmasıdır. Ãyle ki normal Åartlarda bir molekülü oluÅturan atomların tekil enerjisi ortalama olarak eÅittir. Genellikle bir molekülde elektronlar onu oluÅturan atomların çevresine eÅit daÄılır fakat su kimyasında olduÄu gibi bunun istisnaları vardır!
Kuantum su kimyası
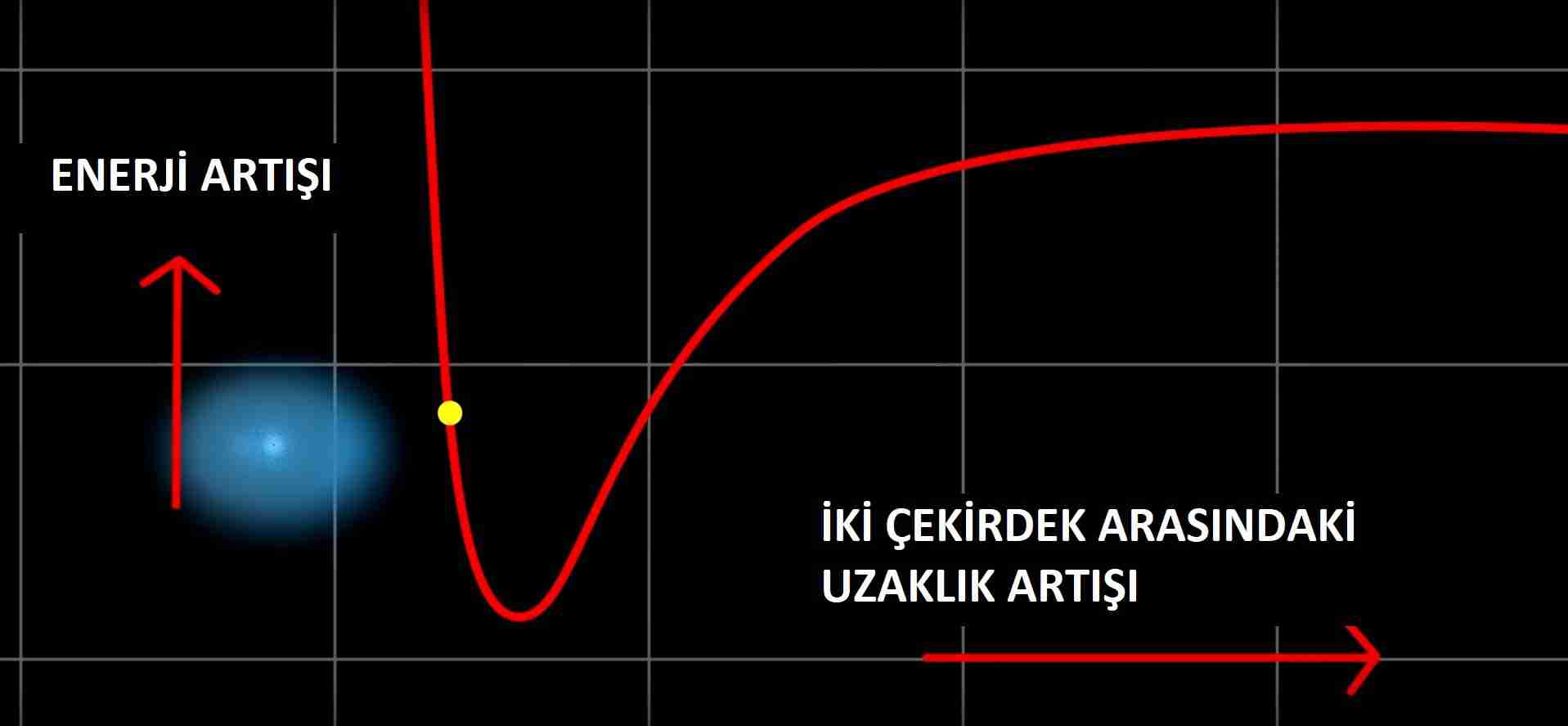
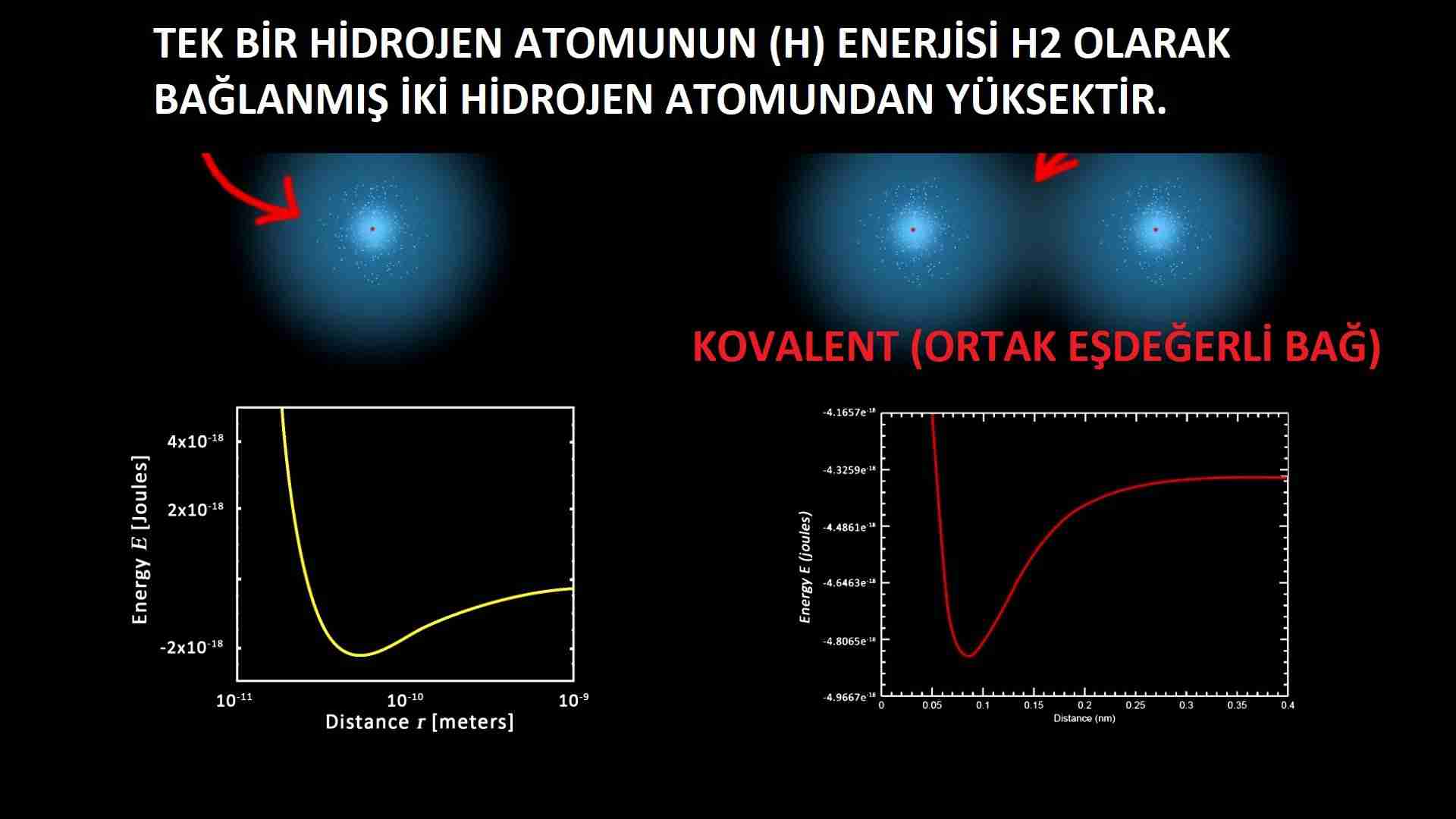
Elektron daÄılımı açısından su moleküllerinin biraz dengesiz olması (resim 5) onların yaÅam denilen bilimsel mucizeyi yaratmasına imkan verir ama biz moleküler hidrojene geri dönelim. Daha anlatacaklarımız var ?: Resim 2 ve 3’teki eÄri grafik çizgisini saÄdan sola izlerseniz atomlar birbirine yaklaÅır ve uzaklaÅırken sistemin potansiyel enerjisiyle kinetik enerjisinin karÅılıklı deÄiÅen düzeyini görebilirsiniz. Grafikteki çukur molekül oluÅturmaya uygun minimum potansiyel enerjidir ve atomlar daha çok buraya çekilir.
Ä°lgili yazı: Zamanda Yolculuk Etmenin 9 Sıra DıÅı Yolu
RESİM 6. Büyütmek için tıklayın.
Kuantum kimya denge iÅidir
Hidrojen atomları uzayda bu yüzden tek tek dolaÅmak yerine moleküler hidrojen oluÅturmaya çalıÅır. Hidrojen atomlarının elektronlarını paylaÅmasıyla da kovalent (eÅdeÄerli) baÄlar oluÅur. Lise kimya derslerinden anımsayabileceÄiniz gibi kararlı molekülleri oluÅturan atomların belirli sayıda elektronları vardır. Bunlar çekirdeÄi soÄan kabuÄu gibi iç içe geçmiÅ elektron kabuklarıyla (yörüngemsiler) sararak elektron bulutları oluÅturur.
Kararlı molekül atomlarının elektron sayısı 2, 10, 18, 36, 54 ve 86 gibidir. Bunlar molekülün minimum potansiyel enerjide olmasını saÄlayan en istikrarlı birleÅimlerdir (Kombinasyon diyecektim ama bu ucubeyi kullanmak istemiyorum. Batılı terimler Fransızca okunuÅuyla yazılır ve birleÅimin Fransızcası kombinezondur. Ä°ngilizcesi kombineyÅın olup kombinasyon bunun radyasyona maruz kalmıŠhalidir).
Her durumda periyodik tablonun en saÄına ve üstüne bakarsanız atıl soy gazları göreceksiniz. Bunlar normal koÅullarda kimyasal tepkimeye girmeyen gazlardır; çünkü elektron birleÅimleri çok kararlıdır. Kendine yeten baÄımsız ruhlu atomlar olup baÅka atomlarla molekül oluÅturmaya sıcak bakmazlar. ?
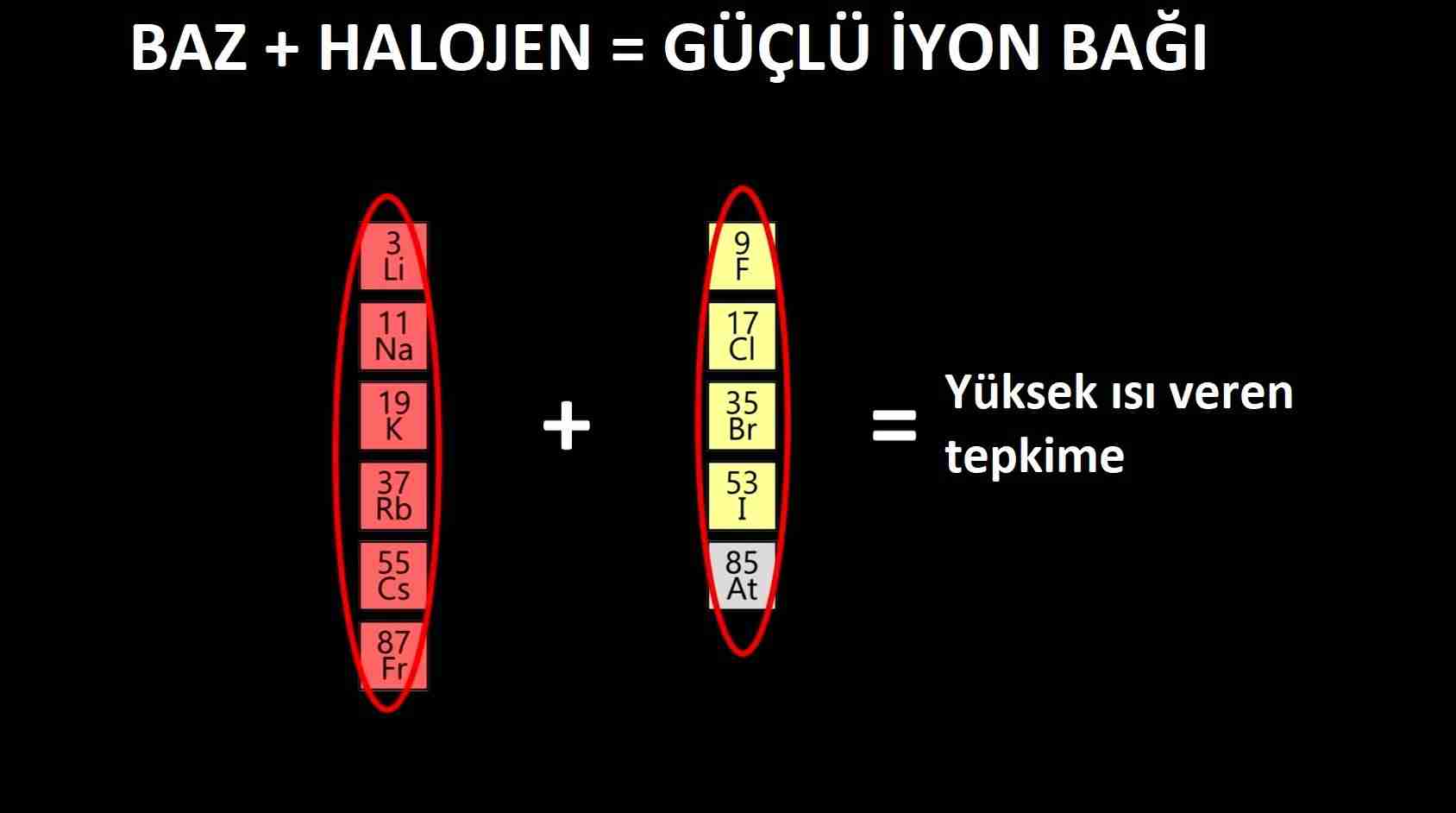
Ãte yandan atıl soy gazların hemen yanındaki halojenlerin kararlı atomlar olmak için bir elektronu eksiktir. Bu yüzden diÄer atomlardan elektron çekerek onlara baÄlanmak isterler. Kısacası halojenler çok reaktiftir. Bazlar ise kararlı atom olamayacak kadar çok elektron içerir ve bunlar da fazla elektronlarını vermek ister. Siz de bazlarla halojenleri bir araya getirirseniz yüksek ısıveren enerjik bir tepkime üretirsiniz (resim 1). Bu iki element grubu ateÅle barut gibidir! ð®
Kuantum kimya ve sofra tuzu
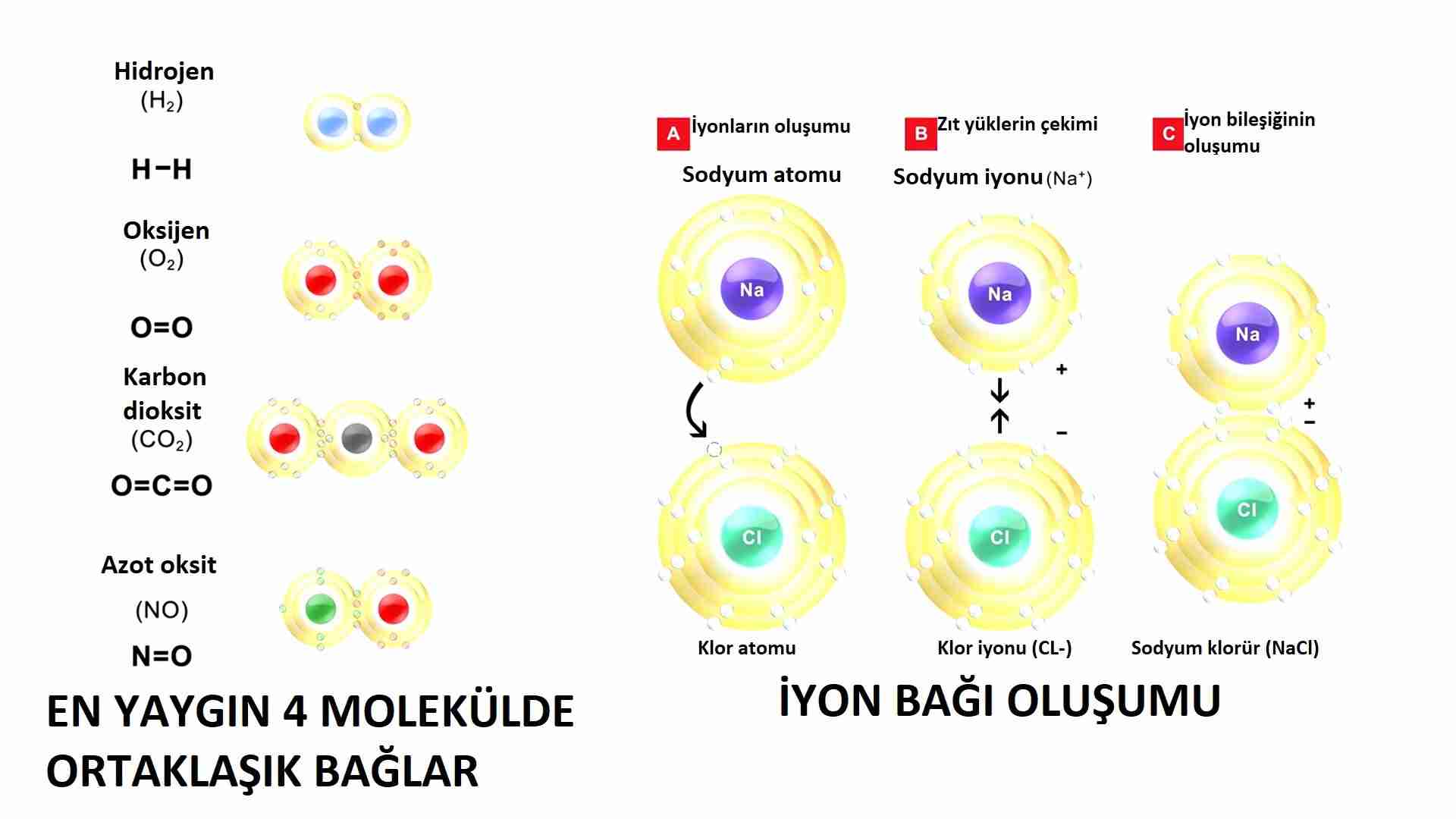
Sonuçta atomlar elektron paylaÅıyorsa kovalent baÄlar, birbiriyle elektron alıÅveriÅi yapıyorsa iyonik baÄlar oluÅur (Resim 6). Halojenler de metal olmayan elementlerle kovalent baÄlar ve metallerle iyonik baÄlar oluÅturur. Kimyasal tepkimeler yaÅamın var olması için çok önemlidir. ÃrneÄin halojen klorür atomu baz metal sodyumla birleÅerek sodyum klorür yani resimdeki gibi bildiÄiniz sofra tuzunu oluÅturur. Tuz kaslarınızla sinirlerinizin elektrokimyasallarla çalıÅması için gerekir ve kan tuzluluk derecesine baÄlı olarak sıvıların dolaÅımını, kan hacmini ve haliyle basıncını düzenler. Peki neden yalnızca belirli sayıda elektronu olan atomlar kararlı moleküller oluÅturur veya Åiddetle tepkimeye girer?
İlgili yazı: Evrenin En Büyük Yıldızı UY Scuti mi?

Sofra tuzu sodyum klorür.
Cevabı kuantum mekaniÄi
Bir moleküler sistemin potansiyel enerjisinin elektromanyetik kuvvete baÄlı 4 bant grafik ekolayzır faktörüyle ve özünde Hamiltonyan ile Schrödinger denklemleriyle belirlendiÄini söyledim. Åimdi potansiyel enerjinin kuantum fiziÄiyle nasıl belirlendiÄini görelim ki iki bileÅen var: Schrödinger denklemi ve Pauli dıÅarlama ilkesi
DıÅarlama ilkesi der ki elektron gibi fermiyon parçacıkları aynı kuantum durumunda var olamaz. Konumuz baÄlamında bu bir yörüngede kendi çevresinde aynı yönde dönen iki elektron olamaz demektir. Bir yörüngede iki elektron varsa biri saat yönünde ve diÄeri de saatin ters yönünde döner. DıÅarlama ilkesi moleküler sistemlerde oyunun kurallarını belirler; çünkü bu ilke atomik yörüngelerdeki elektron sayısını belirler.
Bu sayıyı Schrödinger denklemine ekleyince molekülün minimum enerji düzeyini bulursunuz. ÃrneÄin su molekülünün dıÅarlama ilkesi eklenmiÅ Schrödinger denkleminin Hamiltonyanı resim 5’teki gibidir ama bu denklemler çok karmaÅıktır. Pratikte makul sürede çözmek zordur. Ãzellikle de su gibi sıvılarda tek tek moleküller yerine sıvının kendisiyle hesap yaptıÄımız için (akıÅkanlık vb.).
Böylece Morse yöntemiyle yuvarlak hesap yaparız ve su moleküllerinin potansiyel enerjisini (Morse potansiyeli) resimdeki gibi gösteririz. GrafiÄi meraklısı için koydum fakat detaylı açıklamayacaÄım. Konuda derinleÅmek isteyenler için iyi bir ev ödevi aslında; ama toparlarsak atomların kimyasal baÄlar yoluyla yaÅama izin veren karmaÅık moleküller oluÅturmasının nedeni kuantum mekaniÄidir.
Peki kuantum kimya neden öyledir?
Bunun nedenini bilmiyoruz; çünkü fizik yasalarının var olduÄumuz evreni tanımlaması için gereken parametreleri görelilik ile kuantum alan denklemlerine elle ekliyor ve bunlara evrensel sabit diyoruz. Evrensel sabitlerin neden kendi belirli deÄerine sahip olduÄunu öÄrenene dek kuantum mekaniÄiyle moleküllerin kökenini bilemeyeceÄiz; ancak bu kuantum kimya dalının deÄil, her Åeyin teorisinin araÅtırma alanı. Siz de evrenin bilgi iÅlem kapasitesine bakarak evren simülasyon mu diye sorabilir ve fizikte tanrı var mı sorusunu araÅtırabilirsiniz. SaÄlıklı günlerde keyifli okumalar. ?
Molekül nedir?
1–
2Role of quantum fluctuations in structural dynamics of liquids of light molecules
3A new form of liquid matter: quantum droplets
Daha çok bilim makalesi okumak isterseniz bilim kategorimizi ziyaret edebilirsiniz.
Dizi || Film izlemeyi seviyorsanız Dizi.BuradaBiliyorum.Com sitemizi forumlarla ilgileniyorsanız Forum.BuradaBiliyorum.Com adresini ziyaret edebilirsiniz .



